Hadiah Nobel dalam Kimia pada tahun ini dikongsi oleh trio saintis terkemuka dunia iaitu Michael Stanley Whittingham, John Bannister Goodenough dan Akira Yoshino. Ketiga-tiga saintis ini berhak menerima penghargaan terbesar kerana sumbangan mereka dalam penciptaan bateri ion litium atau LIB (lithium-ion battery).
Keputusan untuk memilih lebih daripada seorang pemenang Hadiah Nobel dalam Kimia pada tahun ini berdasarkan fakta bahawa teknologi ini tidak muncul hasil daripada seorang genius sahaja tetapi melalui penyelesaian masalah yang sistematik.
BESARKAN TEKS A- A+
Kesan besar LIB pada dunia moden
LIB mempunyai kesan yang besar terhadap masyarakat hari ini. Ia menyumbang kepada kewujudan barangan elektronik mudah alih seperti komputer riba dan telefon bimbit. Kini, LIB digunakan untuk menyalurkan kuasa kepada pengangkutan bersih dan rendah karbon seperti kereta elektronik.
Kejayaan LIB ini dijelaskan dengan bagaimana bateri itu berfungsi. Sel bateri melepaskan tenaga daripada tindak balas kimia dalam bentuk elektrik. Sekiranya tindak balas dalamannya kuat, ia boleh menghasilkan voltan yang tinggi.
Bahan-bahan dalam LIB juga tidak memerlukan ruangan yang banyak dan tidak terlalu berat. Ini menjadikan alat ini mempunyai kepadatan tenaga yang tinggi dari segi jumlah dan beratnya.
Litium adalah unsur yang sangat reaktif dan logam paling ringan dalam jadual berkala bahan kimia. Ini adalah sebab utama mengapa LIB menjadi sebahagian teknologi penting dalam dunia elektronik selepas diperkenalkan secara komersial pada awal tahun 1990-an.
Menggunakan litium untuk penyimpanan tenaga elektrokimia seperti bateri pakai buang adalah sesuatu yang mudah sebenarnya. Namun, untuk mencipta bateri yang boleh menyimpan, mengeringkan tenaganya melalui arus elektrik dan memenuhi tenaganya semula apabila dicas adalah sangat sukar.
Penemuan awal bateri ion litium
Profesor Michael Stanley Whittingham
Profesor kimia di Binghamton University, Michael Stanley Whittingham, terlebih dahulu menemukan teknologi LIB. Whittingham menemui teknologi itu ketika dia bekerja sebagai jurutera di Exxon semasa krisis minyak pada tahun 1970-an.
Ketika dunia menghadapi kemungkinan berlakunya kekurangan minyak, syarikatnya melabur untuk membangunkan bateri yang boleh dicas semula. Ketika itu sudah ada bateri seumpama itu tetapi ia sangat besar, berat dan hanya membekalkan tenaga yang sedikit.
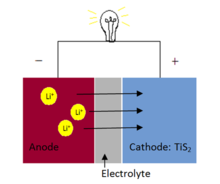
Jika sekeping litium diletakkan di sebelah sepotong TiS₂ (titanum disulfida) dalam bahan yang dikenali sebagai elektrolit, logam itu akan larut dan zarah-zarah yang dicas litium dikenali sebagai ion litium secara spontan akan berpindah dan kekal dalam TiS₂.
Pada masa sama, elektron dipindahkan dari logam litium (elektrod negatif) ke TiS₂ (elektrod positif) membolehkan kita mengeluarkan arus elektrik dari bateri.
Semasa proses cas semula, arus dibalikkan dan litium dipaksa keluar dari TiS₂ dan kembali ke deposit logam. Salah satu keunikan litium adalah ia cenderung untuk membentuk jarum dan dendrit (struktur cawangan panjang) semasa proses mengecas. Ia boleh menyebabkan berlakunya litar pintas dan menjadikan bateri cas semula generasi pertama ini tidak selamat.
Alternatif lebih baik
Profesor John Bannister Goodenough
Pada tahun 1980-an, seorang profesor kejuruteraan mekanikal dari University of Texas, John Bannister Goodenough, telah menemui bahawa litium kobalt oksida adalah alternatif yang lebih baik untuk TiS₂.
Bahan ini juga mengandungi litium tetapi kurang reaktif dengan persekitarannya dan sangat mudah dikendalikan dalam proses penghasilannya. Litium kobalt oksida menjadi "bapa" kepada bahan dalam kebanyakan LIB komersial moden dan membekalkan kuasa kepada telefon bimbit generasi pertama.
Hari ini, kebanyakan elektrod tenaga tinggi yang dasarnya diperbuat dari kobalt sebahagian besarnya digantikan oleh nikel dan mangan (logam rapuh berwarna kelabu keputih-putihan) dalam struktur kristal yang hampir serupa. Ini kerana kobalt sukar ditemui dan tidak begitu efisyen.
Pada penghujung tahun 1980-an, ahli kimia Jepun di Asahi Kasei Corporation, Akira Yoshino, telah membina bateri litium komersial pertama yang boleh dicas semula yang menggunakan grafit (bahan seperti arang) sebagai elektrod negatif.
Dalam binaan baru ini, litium bergerak antara dua struktur hos berbeza, litium kobalt oksida dan grafit. Prinsip ini menyingkirkan penggunaan litium metalik supaya anda tidak membentuk dendrite dan membuatkan LIB lebih selamat digunakan.
Ciptaan baru membekalkan dua kali ganda kuasa
Akira Yoshino
Yoshino juga berhak mendapat penghargaan kerana membangunkan reka bentuk yang membolehkan penggunaan elektrolit organik. Ini memberikan voltan dua kali ganda lebih banyak berbanding menggunakan elektrolit berasaskan air. Namun, aliran elektrolit organik yang lemah bermakna elektrod positif dan negatif mestilah nipis dan diletakkan secara berdekatan.
Yoshino akhirnya menemui cara melapisi bahan elektrod aktif pada logam nipis. Dia berjaya memisahkan elektrod positif dan negatif dengan logam nipis. Dengan ini, generasi pertama LIB mampu bersaing dengan bateri hidrida logam nikel yang menguasai peralatan mudah alih pada awal tahun 1990-an.
Kini, pelbagai penambahbaikkan telah dilakukan pada LIB. Semakin lama, LIB semakin nipis dan kecil tetapi membekalkan kuasa yang lebih banyak berbanding sebelumnya. Suatu hari nanti, penggunaan LIB ini mungkin akan menjadi alternatif utama menggantikan penggunaan kuasa elektrik dan bahan bakar.
Rujukan:
1. Pemenang Hadiah Nobel 2019 dalam bidang Kimia